本研究プロジェクトで整備する動物実験飼育設備、組織培養解析設備の他、平成18年度に整備のクリオスタットなどを用いて、組織培養および動物実験を主な研究手法として加齢・疾患障害の予防治療法の開発を目指す。
リハビリテーション医学は障害のある身体に外部刺激を与え、生体が本来備えている自然治癒力を促し機能回復を促進するものである。一般に適度な外部刺激は身体機能の維持向上を図るものの、弱い刺激では効果はなく、強すぎる刺激は逆に機能障害をきたすことが知られている。身体機能回復を促進する適度な刺激量は、細胞自身の生理的活性を高めると考えられ、細胞機能を活性化するような適用量を踏まえておくことは重要である。障害の機能回復に有効な治療量は、細胞の損傷と修復といった回復メカニズムの解明からも示されるべきであり、リハビリテーション医学で用いるいろいろな治療法の効果は細胞レベルで検証することが重要である。
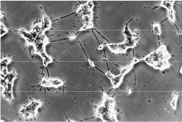
組織培養としては、特殊な細胞内シグナル伝達変異細胞を利用して研究を行う(下図)。代表的な細胞内シグナル伝達変異細胞は神経再生の研究に用いられているラットの副腎髄質褐色細胞腫由来のPC12細胞から得られた、MAPキナーゼ(ERK)経路に作用する神経成長因子には反応しないが、p38経路に働く薬剤や物理刺激で、細胞死ではなく神経分化を起こすという特徴を持つ、MAPキナーゼ経路に変異をきたした特殊な培養神経細胞である。この特異な培養神経細胞は薬剤やリハビリテーションで用いられる様々な物理刺激に鋭敏に反応して、その効果検証を行えるという優れた特性を持っている(Kano et al. Brain research 1026, 302-306. 2004)。この細胞を始め、様々な細胞内シグナル伝達変異細胞を用いて分子生物学的に解析を行うことにより、加齢・疾患障害の予防や治療に効果がある薬剤や物理刺激を見いだすことが可能になる。
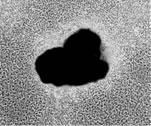
また、我々は各種物理療法の効果を培養細胞と人工骨のハイドロキシアパタイト(Hydroxyapatite, 以下HA)を用いて迅速に調べる方法を開発してきた(Hiragami F, et al. Tiss Cult Res Commun 21:101-107,2002)。すなわち、マウス線維芽細胞を用い物理刺激を与えHAと混合培養すると、HAの周りを囲んだ細胞が立体的に組織形成した三次元様増殖が促進されることを見出し(下図:真ん中の黒いものがHAでその淵で白く光ってみえるのが細胞の重層による三次元様増殖)、この三次元様増殖形成率をパラメータとして各種物理療法の最適条件に関する研究を行ってきた(Hiragami F, et al. Tissue Eng 9:357-364,2003)。三次元様増殖形成のメカニズムについては、これまでの実験結果からp38経路が熱ショックによるアポトーシスを防御するなどの重要な働きをしていることを突き止めた(Hiragami F, at al. J Biomed Mater Res 74:705-711,2005)。
動物実験としてはリハビリテーションで特に問題となる廃用性筋萎縮や関節拘縮・骨粗鬆症についてモデル動物(マウス・ラット)を作成して研究を行う。人の場合には倫理的問題が生じるため、様々な条件設定を行ってリハビリテーションの効果判定を行うことは不可能である。しかし、動物実験では対象をグループ分けして効果検証を行うことが可能になる。最終的には顕微鏡あるいは電子顕微鏡を用いて細胞レベルで検討を行う。


